m1A-seq
項目簡介
N1-methyladenosine(m1A)是一種重要的RNA轉錄後修飾,是RNA分子腺嘌呤第1位氮原子上的甲基化修飾,首次報道是在50多年前【1】。2016 年,何川等人【2】發現m1A對甲基化mRNA的翻譯具有促進作用,存在於多種不同的真核細胞基因轉錄本中,包括酵母菌到哺乳動物,使我們重新認識m1A。越來越多的研究發現,m1A不僅影響局部RNA結構、蛋白-RNA相互作用以及5’UTR的翻譯,還存在於tRNA、rRNA、mRNA和線粒體轉錄本【3】,在維持這些ncRNA的正確結構和功能上發揮重要的作用【4】。m1A修飾的相關研究初露崢嶸,提示我們這個新的 RNA 甲基化修飾有著巨大的研究意義。表觀生物一直專注於表觀遺傳學研究領域,推出 m1A-seq 整體服務,繪製全轉錄組 m1A 甲基化修飾圖譜幫助客戶揭示 m1A 修飾的未知功能與機製。
送樣要求
樣本物種: 僅限人、大小鼠物種,其他物種需評估
≥ 100 μg/ 樣本
總RNA
≥ 3 X107 個細胞 / 樣本
細胞數量
≥ 100 mg/ 樣本
組織
分析內容
基本分析內容
1. 原始數據過濾及質控
2. m1A 的基本特征
• Peak 在基因元件的分布
• Reads 在基因元件的分布
• Peak 關聯基因的特征
3. 參考基因組比對
4. Reads 在染色體上的分布
5. Peak Calling 分析
6. Peak 可視化 差異 Peak 分析
7. Peak 統計分析 差異 Peak 關聯基因 GO,KEGG 分析
8. Motif 分析
高級分析內容
1. RNA-seq 表達差異與 m1A 修飾差異關聯分析
2. m1A 修飾差異與 GWAS 數據庫關聯分析
3. 翻譯組 Ribo-seq 翻譯差異與 m1A 修飾差異關聯分析
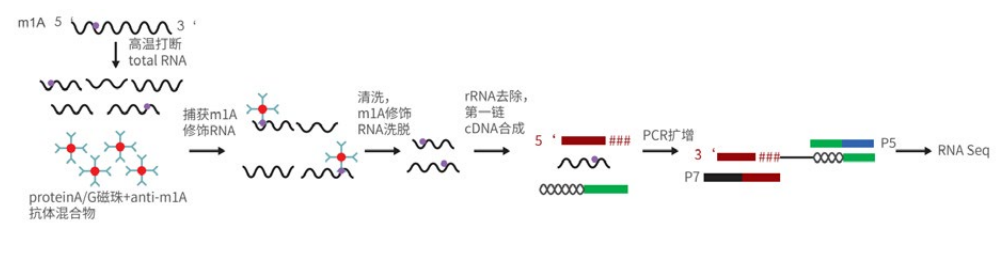
技術原理
將RNA片段化,利用m1A抗體進行免疫沉澱實驗。洗脫RNA片段,反轉錄成cDNA,進行高通量測序。
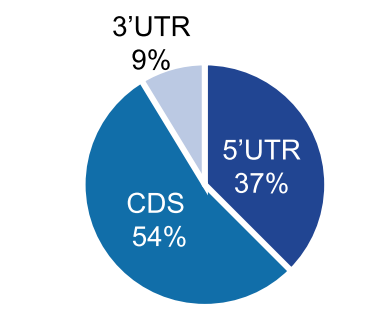
圖1. Peaks 結構百分比圖【2】
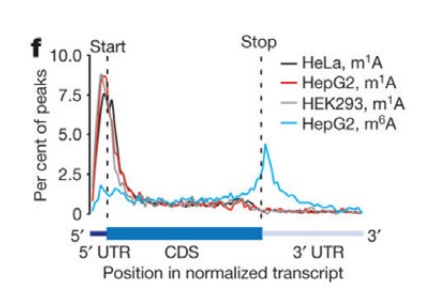
圖 2. m1A修飾位點富集於AUG起始密碼子附近【2】
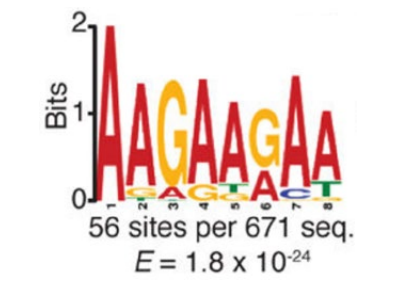
圖3. m1A修飾motif分析【2】

圖4. 某特定基因的m1A修飾區域【2】
客戶文章
PNAS:RNA 修飾通過 ATP5D 調控腫瘤細胞糖酵解 [8]
研究者通過測序和功能研究證實,ATP5D 是 ATP 合成酶最重要的亞單位之一,參與 m1A 去甲基酶 ALKBH3 調節的癌症細胞糖酵解。m1A 修飾的 ATP5D 外顯子1,通過增加與 YTHDF1/eRF1 複合物的結合來負調控其翻譯延伸,從而促進核糖體複合物釋放 mRNA。m1A 還調節 E2F1 的 mRNA 穩定性,E2F1 直接與 ATP5D 啟動子結合,啟動它的轉錄。利用dm1 ACRISPR 係統,靶向 ATP5D m1A,去甲基化,顯著提高了 ATP5D 的表達和癌症細胞的糖酵解。體內實驗證明 m1A/ATP5D 在腫瘤生長和癌症進展中的作用。此研究揭示了 mRNA m1A 修飾和細胞代謝的聯係,對這些相互作用的進一步理解,對癌症治療至關重要。
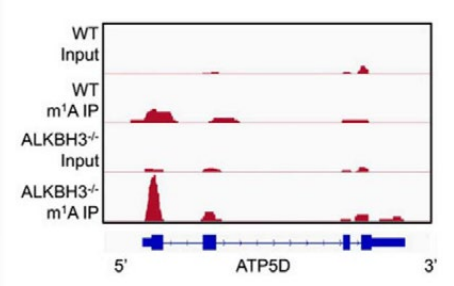
圖5. m1A-seq顯示野生組和ALKBH3-/-HeLa細胞ATP5D基因CDS區的m1A富集峰
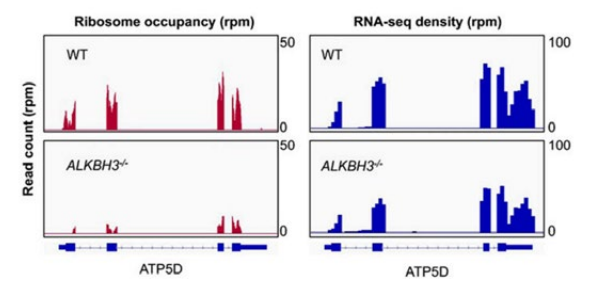
圖6. 兩組細胞的ATP5D基因的mRNA表達水平(RNA-seq) 與核糖體足跡(Ribo-seq)
參考文獻
[1] Maki RA, Brown JL, Cummings DJ. Transfer RNA methyltransferase activity in paramecium aurelia. Biochim Biophys Acta. 1976;425(3):334-341. doi:10.1016/0005-2787(76)90260-4
[2] Dominissini D, Nachtergaele S, Moshitch-Moshkovitz S, et al. The dynamic N(1)-methyladenosine methylome in eukaryotic messenger RNA. Nature. 2016;530(7591):441-446. doi:10.1038/nature16998 [3]Zhang C, Jia G. Reversible RNA Modification N1-methyladenosine (m1A) in mRNA and tRNA. Genomics Proteomics Bioinformatics. 2018;16(3):155-161. doi:10.1016/j.gpb.2018.03.003
[4] Roundtree IA, Evans ME, Pan T, He C. Dynamic RNA Modifications in Gene Expression Regulation. Cell
. 2017;169(7):1187-1200. doi:10.1016/j.cell.2017.05.045
[5] Wu Y, Chen Z, Xie G, et al. RNA m1A methylation regulates glycolysis of cancer cells through modulating ATP5D. PNAS. 2022;119(28):e2119038119. doi:10.1073/pnas.2119038119
